-
Serviços
- Áreas de Prática
-
Setores
- Agribusiness
- Banca e Instituições Financeiras
- Desporto
- Distribuição e Retalho
- Economia Social
- Energia e Recursos Naturais
- Governo e Setor Público
- Imobiliário e Construção
- Infraestruturas
- Mobilidade, Transportes e Logística
- Produção Industrial
- Saúde, Ciências da Vida e Farmacêutico
- Seguros e Fundos de Pensões
- Turismo e Lazer
- Desks
- Buzz Legal
-
Pessoas
-
As nossas pessoas
Meticulosos com o que é. Inconformistas com o que pode vir a ser.
Conheça a equipa
-
-
Conhecimento
-
Subscrever newsletterMantenha-se Informado
Subscreva a newsletter PLMJ para receber informação, alertas e novidades sobre as suas áreas e setores de interesse.
-
-
Sobre nós
-
Candidate-seInvestimos em talento
Procuramos pessoas que vão mais longe, que enfrentam o futuro com confiança.
-
- ESG
-
Serviços
- Áreas de Prática
-
Setores
- Agribusiness
- Banca e Instituições Financeiras
- Desporto
- Distribuição e Retalho
- Economia Social
- Energia e Recursos Naturais
- Governo e Setor Público
- Imobiliário e Construção
- Infraestruturas
- Mobilidade, Transportes e Logística
- Produção Industrial
- Saúde, Ciências da Vida e Farmacêutico
- Seguros e Fundos de Pensões
- Turismo e Lazer
- Desks
- Buzz Legal
-
Pessoas
-
As nossas pessoas
Meticulosos com o que é. Inconformistas com o que pode vir a ser.
Conheça a equipa
-
-
Conhecimento
-
Subscrever newsletterMantenha-se Informado
Subscreva a newsletter PLMJ para receber informação, alertas e novidades sobre as suas áreas e setores de interesse.
-
-
Sobre nós
-
Candidate-seInvestimos em talento
Procuramos pessoas que vão mais longe, que enfrentam o futuro com confiança.
-
- ESG
Nota Informativa
Autorização e revisão de preços dos medicamentos: Critérios a vigorar em 2025
19/11/2024Foi publicada a Portaria n.º 293/2024/1, de 15 de novembro, que procede à definição dos países de referência a considerar em 2025 e define os critérios excecionais a aplicar no regime de revisão de preços dos medicamentos.
Países de referência para novos preços e para a revisão anual de preços
- Pela primeira vez nos últimos 5 anos, ocorre uma alteração nos países de referência para a autorização dos preços dos novos medicamentos e para efeitos de revisão anual de preços dos medicamentos (mercado ambulatório e hospitalar). Os países de referência passam agora a ser Espanha, França, Itália e Bélgica.
Critérios a observar na Revisão Anual de Preços de medicamentos (RAP)
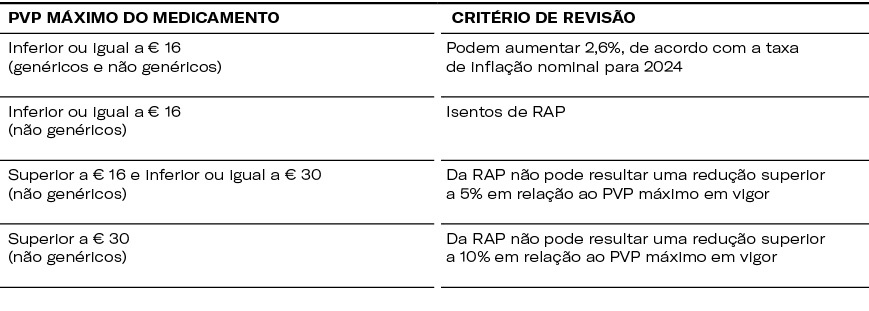
- Mercado Ambulatório

- Mercado Hospitalar (não genéricos e não biossimilares)
- Mercado ambulatório1 e hospitalar (genéricos e biossimilares)
Todos os medicamentos genéricos e biossimilares ficam isentos de RAP, exceto os medicamentos genéricos com preço máximo igual ou superior a € 16 e que seja superior ao preço máximo do medicamento de referência resultante da RAP 2025 ou do aumento de 2,6% (se aplicável), caso em que o preço máximo do medicamento genérico não pode ultrapassar o preço máximo do medicamento de referência.
Prazos de submissão, pelos titulares de AIM ou seus representantes legais, dos preços a praticar em 2025:
- Revisão anual do PVP máximo dos medicamentos não genéricos: Até 15 de dezembro de 2024, com entrada em vigor dos preços no dia 1 de janeiro de 2025;
- Revisão anual do PVP máximo dos medicamentos genéricos e biossimilares: Até 15 de janeiro de 2025, com entrada em vigor dos preços no dia 1 de fevereiro seguinte.
1. Recorde-se que os medicamentos genéricos do mercado ambulatório, com preço inferior ou igual a € 16, podem aumentar até 2,6%.