-
Serviços
- Áreas de Prática
-
Setores
- Agribusiness
- Banca e Instituições Financeiras
- Desporto
- Distribuição e Retalho
- Economia Social
- Energia e Recursos Naturais
- Governo e Setor Público
- Imobiliário e Construção
- Infraestruturas
- Mobilidade, Transportes e Logística
- Produção Industrial
- Saúde, Ciências da Vida e Farmacêutico
- Seguros e Fundos de Pensões
- Turismo e Lazer
- Desks
- Buzz Legal
-
Pessoas
-
As nossas pessoas
Meticulosos com o que é. Inconformistas com o que pode vir a ser.
Conheça a equipa
-
-
Conhecimento
-
Subscrever newsletterMantenha-se Informado
Subscreva a newsletter PLMJ para receber informação, alertas e novidades sobre as suas áreas e setores de interesse.
-
-
Sobre nós
-
Candidate-seInvestimos em talento
Procuramos pessoas que vão mais longe, que enfrentam o futuro com confiança.
-
- ESG
-
Serviços
- Áreas de Prática
-
Setores
- Agribusiness
- Banca e Instituições Financeiras
- Desporto
- Distribuição e Retalho
- Economia Social
- Energia e Recursos Naturais
- Governo e Setor Público
- Imobiliário e Construção
- Infraestruturas
- Mobilidade, Transportes e Logística
- Produção Industrial
- Saúde, Ciências da Vida e Farmacêutico
- Seguros e Fundos de Pensões
- Turismo e Lazer
- Desks
- Buzz Legal
-
Pessoas
-
As nossas pessoas
Meticulosos com o que é. Inconformistas com o que pode vir a ser.
Conheça a equipa
-
-
Conhecimento
-
Subscrever newsletterMantenha-se Informado
Subscreva a newsletter PLMJ para receber informação, alertas e novidades sobre as suas áreas e setores de interesse.
-
-
Sobre nós
-
Candidate-seInvestimos em talento
Procuramos pessoas que vão mais longe, que enfrentam o futuro com confiança.
-
- ESG
Nota Informativa
Espaço Europeu de Dados de Saúde: Revolução Digital na Saúde
26/03/2025A pandemia COVID-19 revelou limitações no intercâmbio e utilização eficiente dos dados de saúde no espaço europeu. Em resposta a estes desafios, a União Europeia adotou um Regulamento que cria o Espaço Europeu de Dados de Saúde (EEDS).
Introdução e contexto regulatório
A pandemia COVID-19 veio revelar importantes limitações no intercâmbio e utilização eficiente dos dados de saúde no espaço europeu. Em resposta a estes desafios, a União Europeia adotou o Regulamento (UE) 2025/327[1], de 11 de fevereiro de 2025 (“Regulamento”), que cria o Espaço Europeu de Dados de Saúde (EEDS). Este diploma estabelece regras ambiciosas sobre o acesso, utilização e partilha transfronteiriça de dados de saúde eletrónicos pessoais.
O EEDS reforça direitos fundamentais previstos no RGPD e introduz novas obrigações para os operadores económicos, enquanto cria uma infraestrutura europeia robusta para intercâmbio de dados de saúde, visando maior eficiência, interoperabilidade e inovação no setor.
Principais pilares e impactos do regulamento
O EEDS assenta sobre 3 pilares fundamentais:
- Melhorar o acesso e o controlo dos cidadãos aos seus dados de saúde:
- Direito de acesso eletrónico gratuito e imediato a dados prioritários (e.g., receitas médicas eletrónicas, relatórios clínicos)[2].
- Direito de inserir e corrigir informações nos seus próprios registos eletrónicos.
- Direito a restringir acessos específicos por profissionais de saúde e visualizar quem acedeu aos seus dados.
- Garantir interoperabilidade[3] transfronteiriça entre sistemas de saúde na UE:
- Obrigação de utilização de formatos comuns europeus para troca de dados.
- Certificação obrigatória (marcação CE) dos sistemas de Registos de Saúde Eletrónicos (Sistemas RSE)[4].
- Facilitar o mercado único digital em saúde, promovendo inovação, investigação e utilização secundária de dados:
- Acesso regulado a dados de saúde para investigação, inovação e formulação de políticas.
- Possibilidade de reutilização secundária dos dados mediante autorização específica.
Cronograma de implementação: aplicação faseada das obrigações
O EEDS entra em vigor a 26 de março de 2025, com aplicação gradual das suas normas devido à complexidade técnica e operacional que a sua implementação acarreta.
Assim:

O EEDS vem estabelecer um regime normativo para o tratamento em formato eletrónico dos dados de saúde[5], facilitando o intercâmbio destes dados entre os prestadores de serviços de saúde localizados nos vários Estados-Membros da EU (formato europeu de intercâmbio de registos de saúde eletrónicos RSE[6]).
No âmbito do EEDS, a UE pretende:
- Criar a infraestrutura transfronteiriça- “A minha saúde @ UE” - que regule a utilização primária, ou seja, aquela relacionada com a prestação de cuidados de saúde.
- Criar a infraestrutura transfronteiriça – “Dados de saúde @ UE” - que regule a utilização secundária, isto é, aquela relacionada com o tratamento de dados de saúde eletrónicos para fins distintos dos originais para os quais foram recolhidos.
- Especificar e complementar alguns direitos das pessoas singulares dispostos no Regulamento (UE) 2016/679 (regulamento geral de proteção de dados - RGPD), procurando consagrar garantias suficientes para proteger a segurança, confidencialidade e uso ético dos dados de saúde eletrónicos pessoais.
Estrutura de governança: novos organismos responsáveis pela implementação e fiscalização
Para a implementação e fiscalização das obrigações decorrentes do EEDS, o regulamento introduz novas entidades institucionais relevantes para os operadores do setor:
- Autoridades digitais nacionais de saúde: responsáveis pela supervisão, implementação do EEDS e garantia dos direitos dos pacientes. Os Estados-Membros devem informar a Comissão sobre a identidade das autoridades de saúde digital até 26 de março de 2027[7]
- Organismos nacionais de acesso a dados de saúde: autorizam e monitorizam pedidos de reutilização secundária dos dados de saúde.
- Órgão europeu do EEDS (EHDS Board): coordena a aplicação coerente do regulamento ao nível da EU, designadamente no que respeita à interoperabilidade transfronteiriça[8].
- Autoridades nacionais de fiscalização do mercado: verificam conformidade técnica e legal dos sistemas RSE colocados no mercado europeu.
Principais obrigações para empresas e operadores económicos
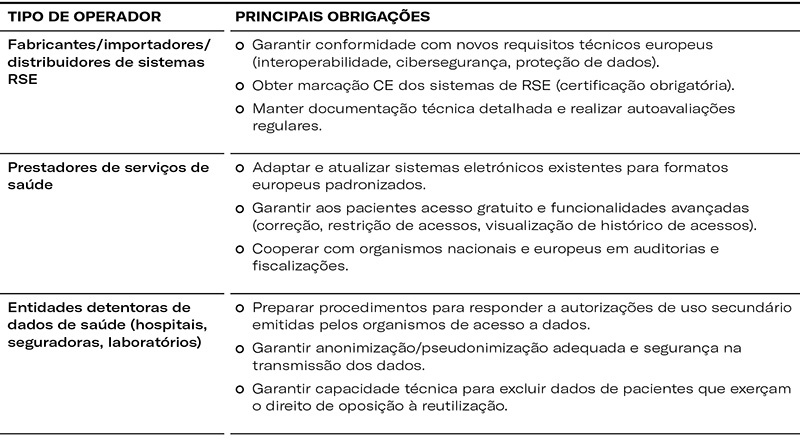
Sanções e riscos por incumprimento
O incumprimento das obrigações impostas pelo EEDS poderá levar à aplicação de coimas administrativas até €20 milhões ou 4% do volume anual global de negócios (o que for maior), à semelhança do RGPD.
Assim, a implementação rigorosa e atempada das novas obrigações deve ser vista como prioridade estratégica, implicando uma gestão rigorosa e uma coordenação operacional eficaz.
Oportunidades estratégicas: inovação, crescimento e competitividade
Além das obrigações legais, o EEDS apresenta importantes oportunidades de negócio:
- Acesso simplificado e regulado a grandes conjuntos de dados europeus pode acelerar inovação, investigação clínica e desenvolvimento de novos produtos.
- Harmonização europeia facilita expansão transfronteiriça de soluções tecnológicas e digitais de saúde.
- Novas infraestruturas digitais oferecem mercados de serviços, aplicações e plataformas tecnológicas de saúde com escala pan-europeia.
Como preparar a implementação: próximos passos
Para assegurar conformidade e aproveitar oportunidades, recomenda-se aos operadores:
- Avaliar sistemas existentes e identificar investimentos necessários para adequação tecnológica.
- Estabelecer políticas internas claras para tratamento, partilha e utilização secundária de dados.
- Formar equipas internas sobre novas regras e nomear responsáveis pela conformidade EEDS.
- Monitorizar ativamente atos de implementação e orientações adicionais da Comissão Europeia, autoridades digitais nacionais e EHDS Board.
Conclusão: um novo paradigma digital na saúde europeia
O regulamento (UE) 2025/327 representa uma transformação digital sem precedentes no setor da saúde na UE. Além da exigência de compliance, constitui uma oportunidade estratégica relevante para entidades do setor da saúde apostarem na inovação digital e beneficiarem de um mercado europeu harmonizado e altamente competitivo.
A implementação bem-sucedida do EEDS exige uma abordagem proativa, informada e estratégica, para enfrentar desafios, aproveitar oportunidades e garantir conformidade total.
Para avaliar a eficácia, pertinência e valor acrescentado do Regulamento, a Comissão realizará avaliações específicas após oito anos, e globais após dez anos desde a sua entrada em vigor, devendo apresentar os relatórios das suas conclusões ao Parlamento Europeu, ao conselho, ao Comité Económico e Social Europeu e ao Comité das Regiões.
[2] Nos termos do artigo 14.º do Regulamento, as categorias prioritárias incluem: (i) resumos de saúde; (ii) receitas eletrónicas; (iii) dispensas eletrónicas; (iv) estudos de imagiologia médica e relatórios de imagiologia conexos; (v) resultados de exames médicos, designadamente resultados laboratoriais e outros resultados de diagnóstico e relatórios conexos; e (vi) notas de alta.
[3] Artigo 2.º alínea f) do Regulamento: interoperabilidade corresponde à “capacidade das organizações, bem como as aplicações informáticas ou os dispositivos do mesmo fabricante ou de diferentes fabricantes, interagirem, através dos processos que apoiam, envolvendo o intercâmbio de informações reconhecimentos, sem alterar o conteúdo dos dados, entre essas organizações, aplicações informáticas ou dispositivos”.
[4] Nos termos do artigo 2.º alínea k) do Regulamento, um sistema de RSE corresponde a “qualquer sistema através do qual o software, ou uma combinação do hardware e do software desse sistema permite que os dados de saúde eletrónicos pessoais que se enquadram nas categorias prioritárias de dados de saúde eletrónicos pessoais previstos no presente regulamento sejam armazenados, intermediados, exportados, importados, convertidos, editados ou visualizados, e destinados pelo fabricante a serem utilizados por prestadores de cuidados de saúde durante a prestação de cuidados de saúde aos doentes ou pelos doentes quando acederem aos seus dados de saúde eletrónicos”.
[5] Os dados de saúde eletrónico abrangem os dados relativos saúde pessoais e genéticos, bem como os dados de saúde que não são pessoais e que foram anonimizados ou que nunca estiveram relacionados com um titular de dados, mas que têm impacto na saúde.
[6] Nos termos do artigo 2.º n.º 2 alínea j) do Regulamento, o RSE corresponde a “um conjunto de dados de saúde eletrónicos relativos a uma pessoa singular e recolhidos no sistema de saúde, tratados para fins de prestação de cuidados de saúde”.
[7] As autoridades de saúde digital designadas nos termos do artigo 19.º do Regulamento devem publicar, de dois em dois anos, um relatório de atividades que contenha uma descrição abrangente das suas atividades. O relatório de atividades deve seguir uma estrutura acordada a nível do Conselho do EEDS.
[8] Nos termos do Regulamento, “O Conselho do EEDS deverá poder emitir contributos por escrito relacionados com a aplicação coerente do […] regulamento em toda a União, nomeadamente ajudando os Estados-Membros a coordenar a utilização de dados de saúde eletrónicos para os cuidados de saúde e a certificação, mas também no que diz respeito à utilização secundária e ao financiamento dessas atividades”.